利益相反管理
- 臨床研究法施行規則 第21条(利益相反管理計画の作成等)
- 臨床研究法における臨床研究の利益相反管理について
(平成30年3月2日医政発0302第1号 厚生労働省医政局研究開発振興課長通知) - 臨床研究法における臨床研究の利益相反管理について
(平成30年11 月30日医政研発1130第17号厚生労働省医政局研究開発振興課長通知)
臨床研究法においては、研究責任医師が利益相反管理の責任を負うことが定められています。 下図に示すように、研究責任医師は利益相反基準を作成し、当該基準に従って研究全体の利益相反の管理計画を 作成し認定臨床研究審査委員に諮ることが求められます。
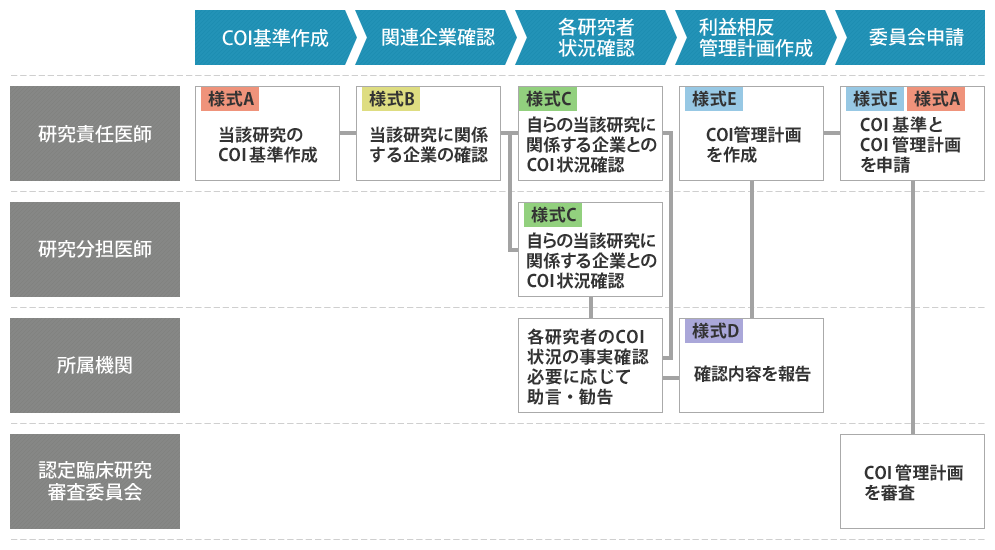
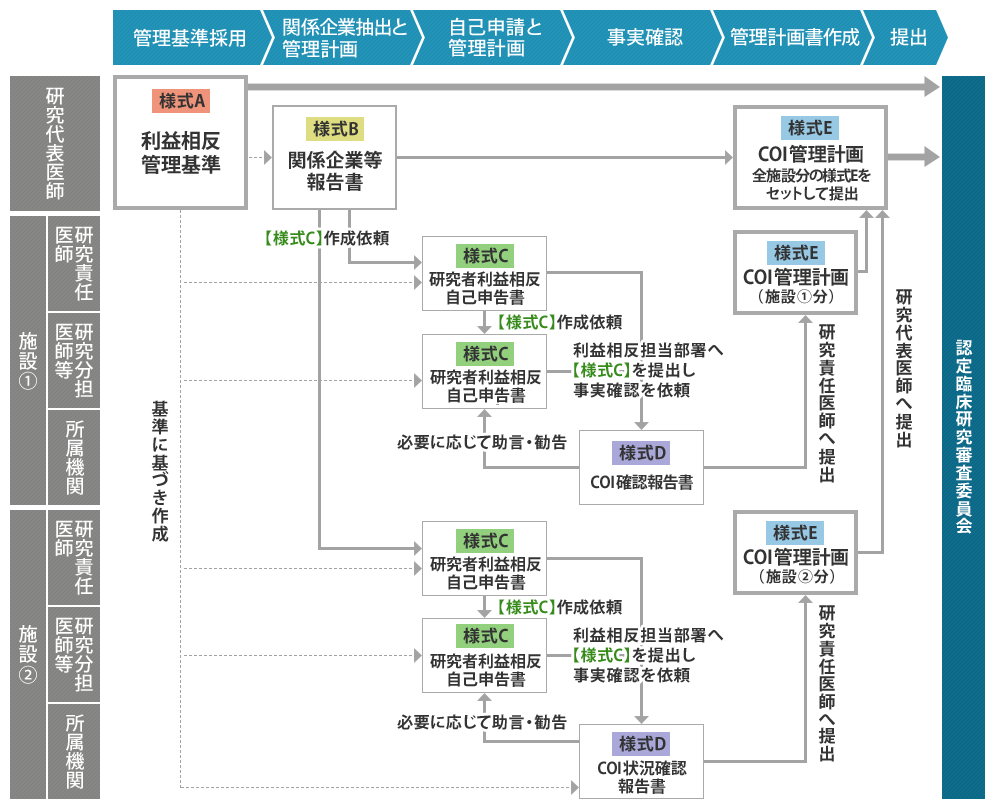
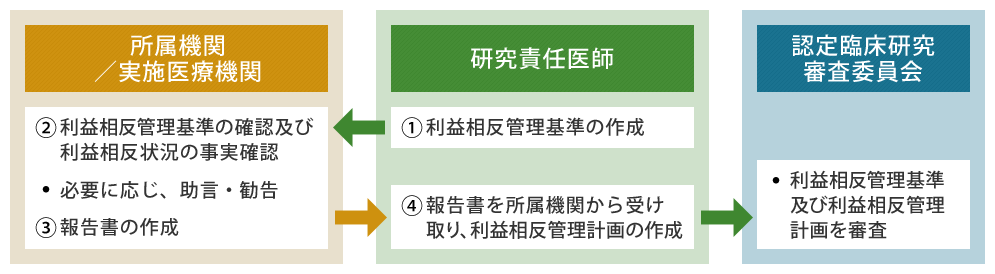
- 研究責任医師または研究代表医師は、当該臨床研究の利益相反管理基準を作成し、当該臨床研究に関わる企業を確認する。
- 研究責任医師・研究分担医師等は、当該臨床研究に関わる企業との利益相反状況を確認し、所属機関が事実確認する。
- 所属機関は、確認内容を研究責任医師へ報告する。
- 研究責任医師または研究代表医師は、所属機関の報告を確認し、当該研究の利益相反管理計画を作成し、当該研究の利益相反管理基準とともに認定臨床研究審査委員会に申請する。
利益相反申告の対象となるのは、
研究責任医師
研究分担医師
統計解析責任者
研究実施によって利益を得る事が明白な者です。
管理が必要となる利益相反は、
研究への企業関与
利益相反申告者と企業との関係の2つです。
1. 研究への企業関与(規則21条1項1号)
研究責任医師(他施設共同研究の場合は研究代表医師)は、実施する臨床研究に関与する企業を抽出し、関係性 を整理して利益相反管理計画を示す必要があります。 以下の要件1~5のいずれかに該当する場合は、企業関与「有り」となります。
- 医薬品等製造販売業者等が製造販売をし、又はしようとする医薬品等を用いる研究
- 医薬品等製造販売業者等からの当該臨床研究に対する研究資金等の提供を受ける場合
- 医薬品等製造販売業者等からの当該臨床研究に使用する物品(医薬品等を含む)、施設等の無償又は相当 程度に安価で提供・貸与を受ける研究
- 医薬品等製造販売業者から無償又は相当程度に安価な価格での役務及び特定役務を受ける研究
- 医薬品等製造販売業者等に在籍している者及び過去2年間在籍していた者が従事する研究
2. 利益相反申告者と企業との関係(規則21条1項2号)
利益相反申告者は、研究対象薬剤等の製造販売業者との関係を申告し、基準に従って管理計画を立て、所属機関にて事実確認を受けることが必要となります。下記事項について、本人及び生計を共にする配偶者、一親等親族の、当該年度と前年度についての申告が必要です。
- 1社からの寄附金が年間200万円以上(寄附金の管理者が報告する)
- 寄付講座所属
- 1社からの個人的利益が年間100万円以上(級と・講演・原稿・コンサル・ライセンス・贈答・接遇等によ る収入)
- 役員等への就任
- 株式保有・出資(株式については、公開株は5%以上、未公開株は1株以上、新株予約権は1個以上)
- その他(寄附講座の受入・特許権を保有している等)
